Erythrozyten im Übermaß: Formen, Diagnostik und Therapie der POLYGLOBULIE.
Der Verdacht gründet meist auf einer Erhöhung von Hämatokrit oder Hämoglobin: Die Polyglobulie bezeichnet eine Vermehrung der Erythrozytenzahl im Blut und wird daher auch Erythrozytose genannt. Für die Diagnose sprechen Hämatokritwerte über 50% bei Männern und über 45 % bei Frauen, ebenso eine Hämoglobinkonzentration über 17 g/dl beziehungsweise 15 g/dl.
Kopfschmerzen, Schwindel oder Tinnitus „ohne Grund“?
Meistens wird eine Polyglobulie im Rahmen einer Routineblutuntersuchung festgestellt, lange bevor Beschwerden in Erscheinung treten. Auch bei Symptomen wie Angina pectoris, chronischen Kopfschmerzen, Schwindel, Tinnitus oder Sehstörungen sollte an eine Hyperviskositätsproblematik gedacht werden. Im Zweifelsfall erfolgt – nach Ausschluss eines Notfalls – eine entsprechende Labordiagnostik.
Formen: Relative oder absolute, primäre oder sekundäre Polyglobulie?
Unterschieden wird eine relative von einer absoluten Polyglobulie. Die relative oder Pseudopolyglobulie bezeichnet eine Erhöhung der Blutdicke durch Flüssigkeitsverlust zum Beispiel im Zuge von Diarrhöen, Erbrechen oder zu starker Entwässerung. Auch eine verminderte Trinkmenge kann zu einer Pseudopolyglobulie führen (anamnestisch und fremdanamnestisch erfragen!).
Die absolute Polyglobulie wird durch eine vermehrte Erythrozytenproduktion ausgelöst und in eine primäre und sekundäre Form unterteilt. Erstere beruht auf einer vom Knochenmark ausgehenden, gesteigerten Produktion von Erythrozyten. Am häufigsten tritt in diesem Rahmen die Polycythaemia vera auf.

Diverse Ursachen von Sauerstoffmangel bis Nierenerkrankung
Die sekundäre Polyglobulie entsteht als Reaktion des Knochenmarks auf eine hormonelle Aktivierung. Diese ist am häufigsten durch Sauerstoffmangel bedingt – man spricht dann auch von reaktiver Polyglobulie –, zum Beispiel infolge von Lungenerkrankungen (COPD, Asthma Bronchiale etc.), Höhenaufenthalten, angeborenen Herzerkrankungen oder Rauchen. Diese führen zu einer gesteigerten Erythropoetinausschüttung in der Niere. Dies gilt auch für eine Nierenarterienstenose mit isoliertem Sauerstoffmangel in der Niere. Zu den weiteren häufigen Ursachen sekundärer Polyglobulien zählen:
- Nierenerkrankungen, die zu einer erhöhten Erythropoetinausschüttung führen (zum Beispiel Zysten, Tumoren, membranöse Glomerulonephritis, Nierentransplantation)
- Tumoren, die eigenständig ektop (außerhalb der Niere)Erythropoetin freisetzen sowie ein mit Tumoren einhergehendes paraneoplastisches Syndrom
- direkte Erythropoetinsubstitution zum Beispiel durch Doping („EPO“) oder therapeutisch bei Leukämien oder Niereninsuffizienz
- Gabe von Blutkonserven zum Beispiel bei Blutdoping
- erhöhte Testosteron- oder Kortisolausschüttung
Somit sind diverse Ursachen, Krankheitsbilder und Organsysteme bei der Abklärung einer Polyglobulie zu berücksichtigen.
Laborwerte bei verschiedenen Formen der Polyglobulie
| Parameter | primäre Polyglobulie | sekundäre Polyglobulie | Pseudopolyglobulie |
|---|---|---|---|
| Hämatokrit | ↑ | ↑ | ↑ |
| Thrombozyten | ↑ | 0 | 0 / ↓ |
| Leukozyten (vor allem Granulozyten) | ↑ | 0 | 0 / ↓ |
| Erythropoetin | 0 / ↓ | ↑ | 0 |
| Sauerstoffpartialdruck (pO2) | 0 | 0 / ↓ | 0 |
| JAK-2-Mutation | + | – | – |
Diagnostik: Hämatokrit, Thrombozyten und Erythropoetin im Fokus
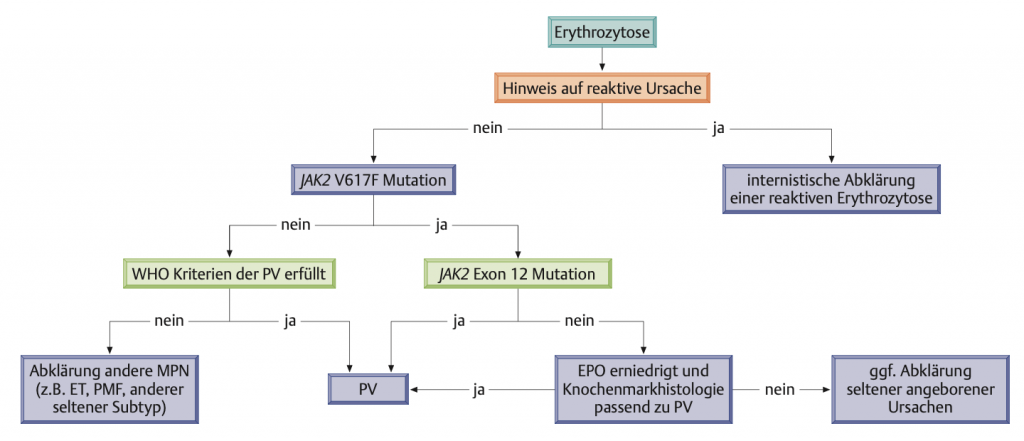
Die Differenzialdiagnostik besteht zunächst einmal in der Erhebung weiterer Laborbefunde. Dazu gehören ein kleines Blutbild, die Erythropoetinkonzentration, der Sauerstoffpartialdruck, eine JAK2-Mutationsanalyse sowie eventuell eine Hämoglobin-Elektrophorese. Eine weitere diagnostische Option stellt die nuklearmedizinische Bestimmung der Erythrozytenmasse dar. Diese wird allerdings in der Praxis kaum noch angewendet.
Wenn der Laborbefund auf eine primäre Polyglobulie hindeutet (siehe Tabelle), folgt im Anschluss eine Abdomensonografie (Splenomegalie) sowie eine Knochenmarkbiopsie (Zeichen erhöhter Erythropoese, Granulopoese und Megakaryopoese).
Diagnose Polycythaemia vera: Hämatokrit, Knochenmark und Gendefekt wegweisend
ür die Diagnose einer Polycythaemia vera als häufigster primärer Form gelten laut WHO die drei Hauptkriterien:
- Erhöhung des Hämatokrits auf über 49 % bei Männern oder über 48 % bei Frauen
- Vermehrung aller drei Zelllinien im Knochenmark, also Steigerung der Erythropoese, der Granulopoese ( Leukozyten↑) und der Megakaryopoese (Thrombozyten↑)
- JAK-2-Mutation (bekannte Punktmutation, die bei vielen myeloproliferativen Erkrankungen auftritt)
- Als Nebenkriterium gilt ein erniedrigter Erythropoetinspiegel.
Zur Diagnosestellung müssen entweder alle drei Hauptkriterien oder die ersten beiden Hauptkriterien und das Nebenkriterium erfüllt sein.
Klinisch zeigt sich bei Patienten mit einer Polycythaemia vera häufig ein durch Wasserkontakt hervorgerufener Juckreiz (aquagener Pruritus). Auch Hyperviskositätssymptome wie Kopfschmerzen oder Schwindel sowie arterielle und/oder venöse Thrombosen sind möglich.
Merke: Aufgrund der Fülle unterschiedlicher Diagnosewege sollten Sie bereits bei der Verdachtsdiagnose einer Polyglobulie beizeiten die Überweisung an einen Hämatoonkologen erwägen und mit dem Patienten besprechen.
Therapie: Aderlass nach ärztlichen Leitlinien
Für eine primäre Polyglobulie sehen auch die ärztlichen AMWF-Leitlinien regelmäßige Aderlässe von 300–500 ml 1- bis 2-mal pro Woche vor sowie niedrig dosiert ASS (Cave: einzelne Polycythaemia-vera-Patienten haben ein erhöhtes Blutungsrisiko, daher ist auf Blutungskomplikationen zu achten). Eine medikamentöse Therapie mit Zytostatika findet nur in seltenen Fällen statt, wenn durch eine Aderlasstherapie keine ausreichende Reduktion des Hämatokrits zu erreichen ist oder es trotz ASS-Gabe zu Thrombosen kommt.
Bei der sekundären Polyglobulie steht die Therapie der Grunderkrankung im Vordergrund. Ist dies nicht zeitnah oder im erforderlichen Umfang möglich, ist auch hier eine Aderlasstherapie zur Senkung des Hämatokrits indiziert. Im Fall einer Pseudopolyglobulie erfolgt lediglich ein Flüssigkeitsausgleich durch Steigerung der Trinkmenge oder Infusion.
Merke: Wenn es unter der Aderlasstherapie zu einem symptomatischen Eisenmangel kommt (MCH, MCV vermindert) kann eine vorsichtige Eisensubstitution nötig sein.
Cave: Sauerstoffmangel als Kontraindikation für Aderlass
Kontraindiziert ist die Aderlasstherapie bei einer reaktiven Polyglobulie, also immer dann, wenn ein Sauerstoffmangel vorliegt. Initial käme es zwar dabei durch die Verminderung der Hyperviskosität zu einer Verbesserung der Symptome. Durch die daraus folgende Reduktion der Erythrozyten stünden allerdings auch weniger Sauerstoffträger zur Verfügung. Die Sauerstoffversorgung würde sich damit weiter verschlechtern. Daher sollten alle Bemühungen auf die Beseitigung der Ursache gerichtet sein. Dies kann zum Beispiel bei angeborener Herzerkrankung den operativen Verschluss eines Septumdefekts bedeuten, das Meiden von Triggerfaktoren bei Asthma bronchiale oder die Beendigung des Tabakkonsums bei COPD. Auch Höhenaufenthalte sollten bei Sauerstoffmangel vermieden werden.
Feinere Diagnostik und Verlaufskontrolle mit dem Doppel-Hämatokrit
In der konventionellen Diagnostik wird ausschließlich der venöse Hämatokrit zur Diagnosestellung herangezogen. Weitgehend unbekannt hingegen ist, dass sich arterieller (kapillar gemessen) und venöser Hämatokrit zum Teil deutlich unterscheiden können: Im Regelfall liegt der venöse Wert um etwa 0,1–1,1% höher als der arterielle. Im von Dr. Peter Hain (Fabian Hains Onkel und Begründer der ganzheitlichen Kardiologie) entwickelten sogenannten Doppel-Hämatokrit wird diese Differenz als V-K-Wert bestimmt. Eine so genaue Messung auch kleinerer Differenzen im Hämatokrit lässt sich nur mithilfe der GoldstandardMethode der Kapillarzentrifugation mit manuellem Ablesen vornehmen. Für die Auswertung benötigt man eine Kapillarzentrifuge und ein Lineal. Genauer beschrieben werden die Methode und Abrechnungsmöglichkeiten im Artikel aus der DHZ 01/2019 „Herz nachts unter Druck“. Eine Sechsfachbestimmung und anschließende Mittelwertbildung erhöht die Genauigkeit zusätzlich. Ein speziell entwickeltes Excelprogramm erlaubt eine einfache und bedienerfreundliche Auswertung der Daten. Außerdem wird hierdurch die differenzierte Betrachtung von Veränderungen im Vergleich zu Voruntersuchungen möglich.Die geringfügig höhere venöse Blutdicke liegt vermutlich darin begründet, dass Flüssigkeit in der Peripherie in das Interstitium (Zellzwischenraum) abgepresst wird. Der Rücktransport erfolgt daraufhin unter Umgehung der Venen über die Lymphe.
Merke: Eine Polyglobulie ist immer durch eine Erhöhung des Hämatokrits im arteriellen und venösen Blut charakterisiert.
Isolierte Erhöhung des venösen Hämatokrits als Fehlerquelle
Zu einer isolierten Erhöhung des venösen Hämatokrits und damit oftmals zu der Fehldiagnose einer Polyglobulie kann es bei erhöhter vegetativer Anspannung kommen: Durch eine gesteigerte Herzfrequenz und/oder -kontraktion steigert sich auch das Herzzeitvolumen und damit die Nierendurchblutung. Weiterhin wird in der Peripherie durch die stärkere Durchblutung mehr Flüssigkeit abgepresst, die über das Lymphsystem – also zunächst außer halb der Venen – transportiert wird. Dies hat eine zunächst auf den venösen Schenkel begrenzte Konzentration des Blutes zur Folge – und damit eine Erhöhung des Hämatokrits. Die genannten Mechanismen sind allerdings lediglich zwei von vielen Faktoren, die eine venöse Konzentrierung erzeugen können. Einige davon sind noch nicht genau bekannt. Zu erkennen ist die isolierte venöse Erhöhung durch eine zeitgleiche Bestimmung des kapillaren (arteriellen) Hämatokrits. Bei stark angespannten Patienten messen wir teilweise Unterschiede von 5% und mehr [2].
Eine isolierte Verminderung des venösen Hämatokrits weist hingegen auf eine Herzinsuffizienz hin. Hierbei wird vermehrt Flüssigkeit im venösen Schenkel zurückgehalten, um so eine bessere Füllung des Herzens und damit eine Kompensation der Leistungsminderung zu erreichen. Bei einem V-K-Wert von 2,1 oder weniger besteht eine hohe Wahrscheinlichkeit für eine Herzinsuffizienz [2].
Fazit: Polyglobulie nie isoliert betrachten
Oftmals ist eine Polyglobulie ein Zufallsbefund, der sich nicht durch vorhergehende Beschwerden äußern muss. Dabei gilt es, die Ursache(n) zu ermitteln und Schein oder Pseudopolyglobulien durch gründliche Anamnese und Doppel-Hämatokrit mit V-K-Wert-Bestimmung auszuschließen. Die Ursachenforschung und Behandlung der eventuell zugrunde liegenden Ursachen steht im Vordergrund der therapeutischen Bemühungen. Alle nicht reaktiven (durch Sauerstoffmangel bedingten), sekundären und primären Polyglobulien lassen sich mit einer Aderlasstherapie naturheilkundlich begleiten.
Die Bestimmung des Erythropoetinspiegels im Blut lässt die Differenzierung zwischen sekundärer, primärer und Pseudopolyglobulie zu. Zu beachten ist, dass die Polycythaemia vera aufgrund der Thrombosegefahr eine potenziell lebensbedrohliche Erkrankung darstellt und daher bei stark erhöhten Hämatokritwerten dringend einer ärztlichen Abklärung bedarf.
Allgemein sollte eine Polyglobulie niemals isoliert betrachtet werden. So spielen in Bezug auf das Thromboserisiko weitere Faktoren wie Alter, genetische Prädisposition, Gerinnungsstörungen, Venenerkrankungen, Herzklappendefekte oder auch Herzrhythmusstörungen eine wichtige Rolle.
Fallbeispiele: Polyglobulie oder nicht?
Anhand der folgenden drei Fallbeispiele lässt sich gut veranschaulichen, wie Anamnese und Diagnostik ineinandergreifen, um bei Verdacht auf eine Polyglobulie zu eruieren, ob und in welcher Form die Erkrankung vorliegt.
Pseudopolyglobulie durch Alkoholkonsum
Patient, 79, stellte sich eigentlich zu einer naturheilkundlichen Begleittherapie einer bekannten arteriellen Hypertonie und Herzrhythmusstörung vor. Anamnestisch berichtete er über einen schon länger bestehenden, gesteigerten Alkoholkonsum. Die Messung zeigte Hämatokritwerte von über 50 % (52,5 % arteriell, 53,1 % venös, siehe Ab- schnitt Doppel-Hämatokrit). Eine explizit diuretische Medikation verneinte er.
Hoher Alkoholkonsum vermindert die ADH- Sekretion (Antidiuretisches Hormon) und steigert somit, ebenso wie eine zu starke medikamentöse Entwässerungstherapie, die Diurese. Mit der Flüssigkeitsausscheidung erhöht sich in beiden Fällen auch der arterielle und venöse Hämatokrit, meist mit einer hohen Differenz zugunsten des venösen Wertes (V-K-Wert + 3 % und mehr). Somit kommt es zu einer Pseudopolyglobulie, die tatsächlich auf Flüssigkeitsmangel und nicht auf einer Vermehrung der Erythrozyten beruht.
Nach einer strikt befolgten Alkoholkarenz zeigte sich innerhalb von vier Monaten eine deutliche Besserung der Hämatokritwerte
auf 46,2 % arteriell und 48,5 % venös. Weitere zwei Monate später waren die Werte auf arteriell 45,4 % und venös 45,2 % gefallen. Auch die Herzrhythmusstörungen und die arterielle Hypertonie hatten sich durch die Alkoholkarenz gebessert.
Die Umkehrung der Differenz beruhte auf einer Herzleistungsschwäche durch einen aktuell vorliegenden Infekt. Nach weiteren vier Monaten ohne Alkoholkarenz kam es zu einer erneuten Erhöhung des Hämatokrits auf arteriell 51,3 % und venös 51,6 %.
Sekundäre Polyglobulie durch dritte Niere
Bei einer Patientin, 65 Jahre, zeigten sich im Rahmen einer Routineuntersuchung leicht erhöhte Hämatokritwerte von 46,9 % arteriell und 47,4 % venös. Die Patientin berichtete über Ohrgeräusche und einen spürbaren Herzschlag. Die Abdomensonografie zeigte eine dritte Niere. Vermutlich kann diese durch eine erhöhte Erythropoetinproduktion eine leichte sekundäre Polyglobulie auslösen. Durch eine kalkulierte Therapie mit kleinen Aderlässen von 50–60 ml alle zwei Wochen sank der Hämatokrit auf Werte unter 45 %. Die Symptomatik verbesserte sich in diesem Zuge deutlich.
V-K-Wert entlarvt Stress hinter Schein-Polyglobulie
Patientin, 71, stellte sich im Rahmen von regelmäßigen Routinekontrollen in der Praxis vor. Im Vorfeld waren bei ihr nie hohe Hämatokritdifferenzen aufgefallen. In der
Untersuchung zeigte sich jedoch ein venöser Hämatokrit von 49,0 %, der für sich stehend den Verdacht auf eine Polyglobulie begründen würde. Der Vergleich mit dem arteriellen Hämatokrit lieferte allerdings einen überraschenden Befund: Dieser lag bei 43,0 %, also 6,0 % (V-K-Wert) unter dem venösen Wert. Ein Messfehler war durch Sechsfachbestimmung und manuelles Able- sen der Werte ausgeschlossen.
Wie war dies zu erklären? In der Folge von starken rheumatischen Schmerzen war es zu einer vegetativen Daueranspannung gekommen, die über einer erhöhte Nieren- aktivität zu einer vorübergehenden venösen Konzentrierung geführt hatte. Ein Anti-CCP- Antikörpernachweis und positiver Rheumafaktor erhärteten den Verdacht auf eine rheumatoide Arthritis. In der Folge rieten wir zur Vorstellung bei einem Rheumatologen. Nach rheumatologischer Therapie mit Rückgang der Schmerzen und damit auch der Anspannung kam es im Verlauf von zwei Wochen bereits zu einer Reduktion des V-K-Wertes auf 4,9 %. Nach weiteren zwei Wochen war die Differenz auf 2,7 % reduziert. Der arterielle Hämatokrit lag nun bei 41,1 %, der venöse Wert bei 43,7 %. Somit bestand nur noch eine geringe Restanspan- nung. Der Hämatokrit lag nun im Normbereich. Der anfängliche Anschein einer Poly- globulie hatte getäuscht.
Autoren: Fabian Hain, Ann-Christin Hain
Quelle: http://dx.doi.org/10.1055/a-1064-6982
Aus „Deutsche Heilpraktiker Zeitschrift“ 01/2020.
Artikel zum Download: https://www.hain-badnauheim.de/wp-content/uploads/2020/03/Praxis_Polyglobulie_Hain_Online.pdf
Weitere Themen
Über uns
In Unserer Praxis betrachten wir den Menschen als Ganzes. Dazu wenden wir zentrale Diagnostik- und Therapieverfahren der sanften Herzmedizin nach meinem Onkel, Dr. Peter Hain, an. Wir kombinieren Schulmedizin und Naturheilkunde und erzielen damit beispiellose Behandlungs- und Therapieergebnisse.